γ-アミノ酪酸 GABA(哺乳類)
- 概要
- 脳内の分布
- 誘導体
- Glu からの生合成と分解(GABA shunt)
- その他の代謝産物からの生合成
- GABA による神経伝達に影響する要因
概要
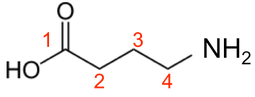
酪酸 CH3-CH2-CH2-COOH の γ 炭素にアミノ基 NH2 がついた物質。
なお,炭素は COOH に結合しているものから順に α,β,γ である。炭素番号は赤の数字で示されている。参考に,生合成の原料となるグルタミン酸 Glu の構造を下に示す。グルタミン酸の C1 が取り去られて GABA ができる。
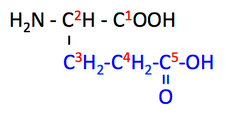
GABA(γ-アミノ酪酸)は代表的な 抑制性神経伝達物質 である。海馬 hippocampus,嗅球 olfactory bulb,小脳プルキンエ細胞に多く存在する。甲殻類では,神経筋接合部の伝達物質として使われる。
GABA はシナプス後膜の GABA 受容体に結合し,Cl- チャネルを開く。これによって細胞外からCl- が流入し,細胞内の電位がさらに低下する。これを過分極という。これによって興奮が伝わりにくくなる。
大脳新皮質のGABAergic neuron
脳には 2 - 5 µmol/g wet tissue 程度存在し,大脳皮質では大部分が GABAergic neuron にある(1)。文献 14 では 1 mM と記載されている。これは Glu や NAA などの主要なアミノ酸に比べて約 1/10 の濃度であり,GABA を正確に定量することは,とくに in vivo ではいまだ難しい。
> グルタミン酸脱炭酸酵素(Glu decarboxylase, GAD)は GABAergic neuron のマーカーとして使われる(2I)。
: GAD+ neuron は,adult rat occipital/parietal/frontal cortex で全ニューロンの 15% 程度。
: Adult rat layer I では,GAD+ neuronの割合が70%以上と高い。深層では 20% 以下ぐらい。
> 大脳新皮質 neocortex における GABAergic neuron の割合は,生物種によって異なる(6)。
: Rodent では,全大脳皮質において15%以下。
: Monkey では,部位によって25%程度。
: ヒトやニホンザル macaque では,layer によっては 34-44% 程度まで増える。
> Rat somatosensory cortex では,GABAergic neuron の約 70% がパルブアルブミン PV を発現(18R)。
: 大脳皮質では,PV はほとんど GABAergic neuron のみで発現する。
: 網膜 retina からの神経やコルチ器では,GABA のない神経でも発現が確認されている。
死後変化 Postmortem changes
> 死後に増える。その増加速度は,脳内のアミノ酸関連物質のなかで最も速い(13R)。
: ラットでは,2 分後に 23% 増え,30 - 60分後に約 2 倍になる。
: ヒトでは増加がやや遅く,30 分後ぐらいから増え始めるが,それでも 60 分後には約 2 倍になる。
: イヌ,マウス,モルモットでも死後に増加するという報告がある。
> 小脳 cerebellum のプルキンエ細胞 Purkinje neuronでは,細胞内濃度は 50 - 100 mM にのぼる(1)。
誘導体 Derivatives
> GABA は脳脊髄液中ではフリーで存在することは少ない(4I)
: His とのジペプチドであるホモカルノシン(11),また2-pyrrolidione (PRDN) としても存在する。
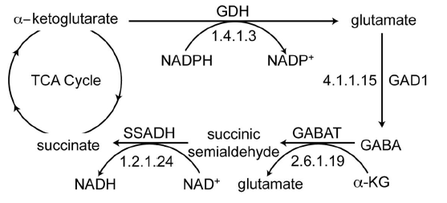
グルタミン酸からの生合成および分解 (GABA shunt)
GABA の生合成および分解を総合的にみると,以下のように TCA 回路のバイパス経路 として考えることができる。この経路は GABA shunt と呼ばれる。
- TCA回路の中間体 α-ケトグルタル酸から酵素 GAD によってグルタミン酸 glutamate が合成される。
- グルタミン酸は,グルタミン酸-グルタミンサイクルで使われるが,一部は GABA に変換される。
- GABA は,GABAT および SSADH によって分解され,最終的にコハク酸として TCA回路 に戻る。
GABA の生合成は主に GABAergic neuron で行われるが,分解は GABAergic neuron と astrocyte の両方で行われる(1)。
> GABAergic neuron では GABA shunt の活性が高く,α-KG のおよそ半分がこちらに流れている(8D)。
グルタミン酸デカルボキシラーゼ glutamate decarboxilase による反応は,以下の図のようになる。NH2 がついている側の CO2 が取り去られる。
なお,グルタミン酸の炭素番号は右から1, 2, 3, 4, 5である。NH2がついているのがC2と覚える。GABAの炭素番号は逆向きになるので,Glu C4 は GABA C2 に対応することになる。

生合成
生合成の原料がどこから来るかという問題
GABA合成の直接の原料は GABAergic neuron の Glu であるが,これがどこから供給されるかという問題がある。そもそもGABAergic neuron ではGluの量が少ない(9I)。さらに,合成酵素GADのKmが0.2 - 1.2 mMであることを考えると,酵素は飽和しておらず,GABAergic neuron内ではGluの供給が律速であると考えられる。
可能性として以下の3経路が考えられ,様々な結果から3が支持されている。
- GABAergic neuron が自前で α-KG から合成したグルタミン酸 Glu。
- Glutamatergic neuron がシナプス間隙に放出したGluを,GABAergic neuron が取り込んだもの。
- Astrocyte がシナプス間隙に放出したグルタミン Gln を,GABAergic neuron が取り込んだもの。
> GABA-T 阻害剤 gabaculin 投与下で,アストロサイトに特異的な[2-13C]-GlcのラベルがGABAに移行(9R)。
分解
GABAergic neuronからシナプスに放出されたGABAは,GABAergic neuron に再び取り込まれるか,もしくはGABA transporter (GAT) を介してastrocyteに取り込まれる(1)。GABAの分解は,GABAergic neuronまたはastrocyteで以下のように進む。
> astrocyteでは,そのままTCA回路を回ってα-KGになり,再びGlu合成に利用されるものもある(9D)。
分解酵素を阻害する実験
> GABA-T 阻害薬ビガバトリン vigabatrin 投与で,GABAの量は約2.5 μmol.gから2-3倍に増える(5)。
: しかし,そのことによるGABA合成速度の低下はみられない。
: Vigabatrin は astrocyte のGABA-Tを効率的に阻害する。
: GABA-Tの活性をgabaculineで完全に阻害すると,合成にも影響するという報告もある。
> SSADH-null mouse では,GABAやその代謝産物γ-hydroxybutyrateが蓄積し,Glu代謝が低下する(8I, 8R)。
その他の代謝産物からの生合成
> プトレシン putrescine などのポリアミンからも合成されるが,adult rat cortexでは全体の1%程度(9D)。
病気との関係
てんかん Epilepsy
> てんかん epilepsy 患者では,CSF (cerebrospinal fluid) や大脳皮質中のGABA量が少ない(4I)。
: CSF中では,大部分のGABAはフリーでなくホモカルノシンや2-pyrrolidinone (PRDN) として存在する。
: ヒト occipital lobe でのPRDN濃度は,in vivo測定で0.2 - 0.3 µmol/g である。
ハンチントン舞踏病 Huntington's chorea (Huntington's disease)
> 脳の特定の領域で GABA 量が低下する(13I)。
統合失調症 Shizophrenia
-> 統合失調症とGABAの詳細へ
統合失調症 schizophrenia では,GABA の量が大脳皮質 cortex や海馬 hippocampus で低下するのが一般的である。
GABA が低下している脳領域では,グルタミン作動性ニューロン等の活性が上昇する。そのため,脳のネットワークがうまく機能しなくなり,認知能力の低下や幻覚などの症状を引き起こすものと考えられている。
> うつ病 depression,アルコール中毒患者などでも脳内のGABA量に異常がみられる(3)。
GABAによる神経伝達に影響する要因
> ベンゾジアゼピンは,GABA 受容体に結合して中枢神経の活動を抑制する薬品である(10)。
: 抗不安薬,睡眠薬として用いられている。
> エタノールもGABA受容体と結合し,中枢神経を抑制する作用をもたらす(10)。
: ベンゾジアゼピンとは結合部位が異なる。併用は効果が増強されるので望ましくない。
: エタノールは,同時にエンドルフィンやセロトニンの分泌も促進する。
> グルタミン酸から GABA を合成する GAD は,ビタミンB6を補酵素とする(10)。
: ビタミンB6が不足すると,中枢神経の興奮が収まらずにけいれんが生じることがある。
低酸素
> 爬虫類(カメ)や魚類では,低酸素または無酸素 anoxia 状態で脳内の GABA が増える(15I, 15R)。
: グルタミン酸などの興奮性神経伝達物質は減り,脳のエネルギー消費が低下する。
References
- Behar 2004a (Book). Ed. Shulman and Rothman. "Brain Energetics & Neuronal Activity". Chapter 6.
- Beaulieu 1993a. Numerical data on neocortical neurons in adult rat, with special reference to the GABA population. Brain Res, 609, 284-292.
- de Graaf et al. 2003a (Review). In vivo 1H-[13C]-NMR spectrometry of cerebral metabolism. NMR Biomed 16, 339-357.
- Hyder et al. 1999a. Localized 1H NMR measurements of 2-pyrrolidinone in human brain in vivo. Magn Reon Med 41, 889-896.
- de Graaf et al. 2006a. Acute regulation of steady-state GABA levels following GABA-transaminase inhibition in rat cerebral cotex. Neurochem Int 48, 508-514.
- Defelipe 2011a (Review). The evolution of the brain, the human nature of cortical circuits, and intellectual creativity. Front Neuroanat 5, 29.
- Ippolito et al. 2006a. Linkage between cellular communications, energy utilization, and proliferation in metastatic neuroendocrine cancers. PNAS 103, 12505-12510.
- Chowdhury et al. 2007a. Altered cerebral glucose and acetate metabolism in succinic semialdehyde dehydrogenase-deficient mice: evidence for glial dysfunction and reduced glutamate/glutamine cycling. J Neurochem 103, 2077-2091.
- Patel et al. 2001a. Glutamine is the major precursor for GABA synthesis in rat neocortex in vivo following acute GABA-transaminase inhibition. Brain Res 919, 207-220.
- 河合良訓 監修 2005a. 脳単. 株式会社エヌ・ティー・エス.
- Perry et al. 1981a. Postmortem changes in amino compounds for the liberation of GABA in human and rat brain. J Neurochem 36, 406-412.
- Govindaraju et al. 2000a. Proton NMR chemicha shifts and coupling constants for brain metabolites. NMR Biomed 13, 129-153.
- Perry et al. 1981a. Postmortem changes of amino compounds in human and rat brain. J Neurochem 36, 406-412.
- Yang et al. 2005a. In vivo detection of cortical GABA turnover from intravenously infused [1-13C]D-glucose. Magn Reson Med 53, 1258-1267.
- Lardon et al. 2005a. 1H-NMR study of the metabolome of an exceptionally anoxia tolerant vertebrate, the crucian carp (Carassius carassius). Metabolomics 9, 311-323.
- Gill et al. 2011a. A novel α5GABAAR-positive allosteric modulator reverses hyperactivation of the dopamine system in the MAM model of schizophrenia. Neuropsychopharmacology 36, 1903-1911.
- Lodge et al. 2009a. A loss of parvalbumin-containing interneurons is associated with diminished oscillatory activity in an animal model of schizophrenia. J Neurosci 29, 2344-2354.
-
Celio 1986a. Parvalbumin in most gamma-aminobutyric acid-containing neurons of the rat cerebral cortex. Science 231, 995-997.