アミノ酸 構造式の覚え方
2018/02/11 更新
ここは,タンパク質構成アミノ酸 20 種の構造を覚えるためのページです。
私が使った覚え方を載せてあるだけで,「アラニン系」など必ずしもアミノ酸の生化学的特徴を反映しない言葉がたくさん出てくるので,目的を間違えずにご利用下さい。
アミノ酸構造式の覚え方
- アミノ酸基本構造
- まずは単純な Gly, Ala から
- アラニン系アミノ酸
- 名前がそのままのフェニルアラニン
- Phe の次はサシスセソ
- 冥王リンチ: 硫黄のメチオニン,リン酸化のチロシン
- 分岐鎖アミノ酸は勢いで
- 「酸」 がつくもの,つかないもの
- 側鎖の長い Long Amino acid (Lys, Arg)
- 丸いヒップは仲間外れ(環状の His, Pro)
- トリはトリプトファンで
アミノ酸の基本構造
最初に,アミノ酸の基本構造を理解しよう。
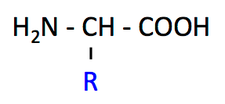
タンパク質構成アミノ酸は,右の図のようにアミノ基 -NH2 とカルボキシル基 -COOH の両方が一つの炭素(これを α 炭素 という)に結合している。
α 炭素に様々な側鎖(R,このページでは青字で示す部分)が結合しており,側鎖によってアミノ酸の性質が決まる。つまり,アミノ酸の構造を覚えるとは,側鎖 R の構造を覚えるということになる。
なお,アミノ酸は中性付近の水溶液中では COOH が COO- に,NH2 が NH3+ になり,両性イオンとして存在している。
このページの内容は,Berg の Biochemistry などを参考にしています(ページの一番下,文献 2)。
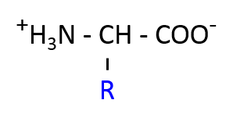
まずは単純なグリシン,アラニンから
まずは,単純な グリシン Gly と アラニン Ala を覚えよう。グリシンは側鎖が H,アラニンは CH3 だ。グリシンには アミノ酢酸 という別名もある。酢酸 CH3COOH にアミノ基 NH2 がついているということ。
グリシン, Gly, G

アラニン, Ala, A
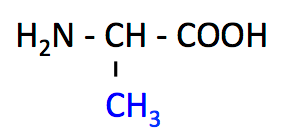
アラニン系アミノ酸 : 名前そのままのフェニルアラニン
アラニンを基本に,CH3 にちょっと付け足しただけのアミノ酸がいくつかある。
ベンゼン環をつけてみたのが フェニルアラニン Phe。「フェニル」はフェニル基 phenyl group C6H5- なので,まさにそのままの名前だ。
C の 4 本の手の一本がベンゼン環との結合に使われるので,アラニンの CH3 はもちろん CH2 になる。
追記(2018/02/11):
フェニル基を C6H6- と書いてしまっていました。正しくはC6H5- です。お詫びして訂正致します。
フェニルアラニン, Phe, F

アラニン系アミノ酸: Phe の次はサシスセソ
システイン Cys は髪の毛に多く含まれているアミノ酸である。髪の毛を燃やすと変な匂いがするが,それは硫黄 S に由来する。アラニンの H のかわりに,硫黄を含む SH をつけたのがシステインである。
この SH 基は S-S 結合という結合を作ることができる。これは,タンパク質の立体構造の形成などに重要な役割を果たしている。
システイン, Cys, C
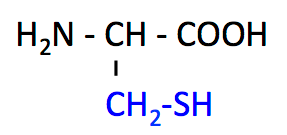
セリン, Ser, S

スレオニン(トレオニン), Thr, T
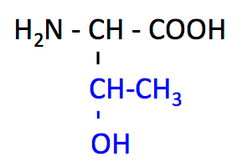
冥王リンチ: 硫黄つながりでメチオニン,リン酸化つながりでチロシンを覚える
システインの他に,もう一つ硫黄 S を含むアミノ酸がある。開始コドンにコードされる メチオニン Met である。システインが少し長くなったような構造だが,側鎖の炭素数も増えているので,単純に SH を S-CH3 にしないように注意する。
メチオニンで硫黄,リン酸化でチロシンなので,合わせて 冥王リンチ と覚える。
メチオニン Methionine, Met, M
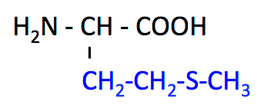
チロシン, Tyr, Y

分岐鎖アミノ酸
次は,側鎖に枝分かれがある分岐鎖アミノ酸(BCAA; branched-chain amino acids)。これを覚えるために,この人に登場して頂く。

バリン Valine, V

イソロイシン Ile は,ロイシンの分岐鎖部分の CH3 が側鎖の根元に寄ってきたものである。
つまり,バリン・ロイシン・イソロイシンという順番も覚えるために都合が良い。さすがである。ちなみに,バリン ロイシン イソロイシン で検索すると,予測変換にアカギと出てくる。実は有名な場面なのかもしれない。
ロイシン Leucine, Leu, L
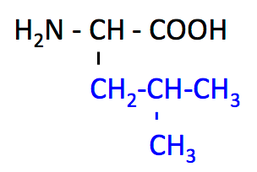
イソロイシン, Ile, I

なお,この長い炭化水素側鎖のために,分岐鎖アミノ酸はいずれも疎水性が強い。そのため,タンパク質の表面には位置しにくく,内側に折りたたまれる傾向がある。側鎖のパターンが異なっていることは,タンパク質内部で複雑に絡まりあい,全体としてコンパクトな構造をとるためにも役立っている。
「酸」 がつくもの,つかないもの
アスパラギン酸 Aspartate, aspartic acid, Asp, D
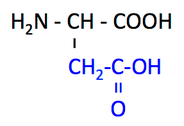
アスパラギン Asparagine, Asn, N
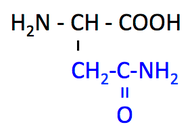
グルタミン酸 Glutamate, glutamic acid, Glu, E
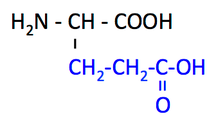
グルタミン Glutamine, Gln, Q
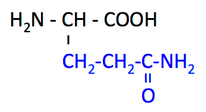
構造式をみると,すぐに以下のような重要かつシンプルなポイントがあることがわかる。
なお,「酸性アミノ酸」と言った場合,このグルタミン酸とアスパラギン酸を指す。電子の授受は電荷の変化をもたらすので,酸性・塩基性アミノ酸 = 荷電アミノ酸でもある。
少し専門的になるが,関連するトピックをいくつか挙げておこう。
- アスパラギンは,アスパラガスの汁から単離されたためにこの名前がつけられた。1806 年のことで,最初に単離されたアミノ酸である。
- グルタミン酸からのグルタミン合成は,OH を取り去ってアンモニウムイオン NH4+ を付加する反応であり,グルタミンシンセターゼ glutamine sythetase という酵素に触媒される。これは アンモニア解毒機構 の一つである。
酸・塩基,解離定数,pH,緩衝液(バッファー)あたりが不安な人は,右のリンク先を参照のこと。
酸・塩基関係は,この順に読むとわかりやすいです。
その他基礎的事項
側鎖の Nagai Long Amino acid (Lys, Arg)
リジン Lysine, Lys, K
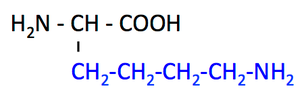
アルギニン Arginine, Arg, R
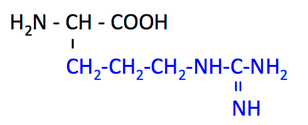
どちらも CH2 の長い側鎖 とアミノ基 NH2 をもつこと が特徴である。やや無理矢理であるが,長いをローマ字表記で Nagai として,NH2 のことを思い出すヒントにする。下に出てくる尿素 Nyouso の N と考えても OK。
リジンは比較的シンプルな構造だが,アルギニンは側鎖の先端部の NH に囲まれた C が特徴である。 この部分は,尿素回路で 尿素を作るために使われる ことを知っていると,なぜこんな構造をしているのか理解しやすいだろう。
生成するアミノ酸であるオルニチン ornithine (Orn) はタンパク質を構成しないアミノ酸であるが,リジンにとても構造が似ている。せっかくなので,頭の片隅に置いておこう。この反応は,アルギナーゼ arginase (EC 3.5.3.1) という酵素に触媒される。

丸いヒップは仲間外れ(His, Pro)
ヒップ hip で覚える ヒスチジン His と プロリン Pro は,どちらも他のアミノ酸がもたない構造を含む仲間外れのアミノ酸である。
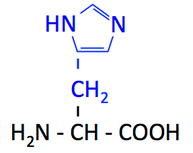
ヒスチジンの側鎖は N を 2 つ含む五員環をもっており,これには イミダゾール基 imidazole group という名前が付いている。正に荷電する性質をもち,電子の受け渡しに関与することができるので,酵素の活性中心になりやすいアミノ酸である。
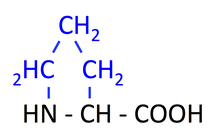
プロリンは,C と H で構成された環状構造をもっており,これによって本来アミノ酸のアミノ基であるはずの NH2 が NH になっている。したがって,正式にはアミノ酸ではない。
ヒスチジン Histidine, His, H
プロリン Proline, Pro, P
*2016/7/15 に間違いを修正しました。今まで見て頂いていた皆様,すみませんでした。
トリはトリプトファンで!
トリプトファン, Tryptophan, Trp, W



管理人 (火曜日, 31 10月 2023 16:50)
アタカマ様
トリプトファン修正いたしました。コメントありがとうございました!
アタカマ (土曜日, 17 7月 2021 18:26)
トリプトファンの綴りはtryptophanではないでしょうか
管理人 (水曜日, 13 3月 2019 09:51)
大学生様
リジンの一文字略称、修正しました。ご指摘ありがとうございました!
大学生 (水曜日, 13 3月 2019 01:39)
別のページですがリジンの一文字略称が間違っており、KではなくLになっています。Lはロイシンだと思います。
管理人 (土曜日, 10 2月 2018 09:35)
受験生様
ご指摘ありがとうございました。C6H5です。訂正しましたのでご確認下さい。今後ともよろしくお願いします!
受験生 (金曜日, 09 2月 2018 07:17)
フェニルアラニンの説明部分でフェニル基をC6H6と表記されていますが、C6H5ではないでしょうか。確認お願いします。
管理人 (金曜日, 15 7月 2016 09:30)
ご指摘ありがとうございました。お恥ずかしい限りです・・・ 構造式修正しました。
薬学生 (火曜日, 12 7月 2016 04:11)
とても参考になりました!
プロリンの構造式だけ水素がバラバラです笑
管理人 (月曜日, 27 7月 2015 18:09)
コメントありがとうございます。覚えるのは難しいですよね。ちょっと更新したので,よろしければご参考にしてみて下さい。
Licht (火曜日, 07 7月 2015 07:01)
書いても覚えられませんでしたが、覚えるべき順番が提示されているので、参考にしたいと思います
管理人 (日曜日, 08 3月 2015 07:49)
ありがとうございます! 今後ともよろしくお願いします。
金子 (木曜日, 11 12月 2014 00:57)
すばらしい! 何年経っても覚えられないものが、とても便利です!!